А.И. Горбатенко, Н.О. Костяная, 2016
Применение обогащенной тромбоцитами аутоплазмы в комплексной терапии остеоартроза коленных суставов.
Вестник травматологии и ортопедии имени Н.Н. Приорова. 2016. №2. С. 40-45.
Проведена оценка эффективности использования обогащенной тромбоцитами аутоплазмы (ОТП) в лечении остеоартроза. В проспективное исследование включено 120 человек (83 женщины, 37 мужчин, средний возраст 52,8±4,5 года) с остеоартрозом коленных суставов II–IV стадии по классификации Kellgren — Lawrence, установленным клинико-рентгенологическим путем. Пациентам основной группы (n=60) был проведен курс внутрисуставных инъекций ОТП (3 инъекции с интервалом 1–2 нед). В контрольной группе (n=60) пациенты получали курсами нестероидные противовоспалительные средства (НПВС), а также периодически по показаниям инъекции глюкокортикостероидов. Результаты оценивали по вербальной шкале эффективности лечения, шкале Лекена, визуально-аналоговой шкале боли. Срок наблюдения составил 6 мес.
Применение ОТП позволило уменьшить выраженность болевого синдрома, улучшить функцию коленного сустава в отсутствие нежелательных явлений. Доля пациентов, отметивших эффективность лечения по прошествии 6 мес, в основной группе оказалась на 31% больше, чем в контрольной. Полученные данные позволяют рекомендовать использование ОТП в лечении остеоартроза коленных суставов как альтернативу НПВС, особенно при наличии противопоказаний к последним.
Use of Platelet-Rich Autoplasma in Complex Therapy of Knee Osteoarthrosis
A.I. Gorbatenko, N.O. Kostyanaya
Rostov State Medical University; Rostov-on-Don, Russia
Efficacy of platelet-rich autoplasma (PRA) in treatment of osteoarthrosis was evaluated. Prospective study included 120 patients (83 females, 37 males, mean age 52.8±4.5 years) with clinical and roentgenologic diagnosis of II-IV stage osteoarthrosis by Kellgren-Lawrence classification. The patients from the main group (n=60) were on courses of PRA intraarticular injections (3 injections with 1-2 weeks interval). In the control group the patients received nonsteroidal anti-inflammatory drugs (NSAIDs) and periodically injections of glucocorticoids when indicated. Results were assessed by the verbal efficacy scale, Lequesne index and the pain visual analog scale. Follow up period made up 6 months.
Use of PRA enabled to eliminate pain syndrome and improve knee joint function without adverse effects. In 6 months the number of patients who noted the efficacy of treatment was 31% higher in the main group than in the control one. The obtained results allow recommending PRA use for knee osteoarthrosis treatment as an alternative to NSAIDs especially in contraindications to the latter.
Введение
Остеоартроз — хроническое прогрессирующее заболевание синовиальных суставов с поражением, прежде всего, гиалинового хряща и субхондральной кости в результате взаимодействия сложного комплекса биомеханических, биохимических и/или генетических факторов [1]. Прогрессирование заболевания приводит к потере хряща и сопутствующему поражению других компонентов сустава (синовиальная оболочка, связки) и является одной из основных причин преждевременной потери трудоспособности и инвалидности у лиц молодого возраста [2], а также хронического болевого синдрома, снижающего качество жизни лиц пожилого и старческого возраста [3].
Остеоартроз лидирует по распространенности среди других ревматических болезней. В последние годы наблюдается отчетливая тенденция к увеличению частоты остеоартроза в популяции, что во многом связано с увеличением продолжительности жизни населения [1] и числа людей, активно занимающихся спортом [4]. «Золотым стандартом» лечения остеоартроза коленных суставов на настоящий момент является базовая схема, предложенная на заседании ESCEO [5], в которую входят анальгетики, нестероидные противовоспалительные средства (НПВС), глюкокортикостероиды, хондропротекторы и корректоры метаболизма хрящевой ткани или симптоматические препараты замедленного действия (SYSADOA), препараты гиалуроновой кислоты и в конечном итоге — эндопротезирование. Однако НПВС, анальгетики, глюкокортикостероиды, которые применяются в основном для купирования болевого синдрома, оказывают побочное действие на различные органы и системы, особенно при длительном применении. В связи с этим поиск новых, безопасных методов лечения остеоартроза коленных суставов является актуальной задачей. Одним из таких способов является применение обогащенной тромбоцитами аутоплазмы (ОТП) [6].
Использование регенеративных возможностей ОТП в лечении травматических дефектов и дегенеративно-дистрофических изменений суставного хряща представляет особый интерес, так как гиалиновый хрящ характеризуется крайне низкой способностью к спонтанной регенерации [7]. Обогащенная тромбоцитами аутоплазма является наиболее доступным, простым и недорогим источником факторов роста [8, 9]. В последнее время был опубликован ряд работ по оценке эффективности применения ОТП по сравнению с вискосапплементарной терапией [10–12], с инъекциями глюкокортикостероидов [13]. Несмотря на возрастающую популярность данного метода и большое число положительных отзывов, до сих пор нет единого подхода и выработанной методики применения ОТП для лечения остеоартроза коленных суставов.
Цель исследования: оценить эффективность применения ОТП в комплексной терапии остеоартроза коленных суставов и сравнить ее с эффективностью терапии НПВС.
Пациенты и методы
На базе клиники РостГМУ проведено проспективное исследование, в котором приняли участие 120 человек (83 женщины, 37 мужчин, средний возраст 52,8±4,5 года, средний индекс массы тела 30,22±1,4) с остеоартрозом коленных суставов II–III, III и III–IV стадии по классификации Kellgren —Lawrence, установленным клинико-рентгенологическим путем. Критерием исключения из исследования был диагноз «ревматоидный остеоартроз», подтвержденный рентгенологическими и биохимическими данными.
Пациенты были отобраны случайным образом и разделены на две группы в зависимости от получаемого лечения (табл. 1). Группы были сопоставимы по возрасту, ИМТ, соотношению мужчин и женщин, и количеству пациентов, страдающих односторонним и двусторонним поражением коленных суставов.
| Характеристика | Основная группа | Контрольная группа |
| Возраст, годы | 49,8±5,2
(16–79) |
52,9±4,5 (22–80)* |
| Пол, м/ж | 19/41 | 18/42 |
| ИМТ | 27,8±1,4 (18,22–42,24) | 30,1±1,4* |
| Одностороннее поражение | 50 | 46 |
| Двустороннее поражение | 10 | 14 |
* p<0,05.
В обеих группах комплексное лечение остеоартроза коленных суставов проводилось согласно рекомендациям ESCEO [5], однако в основной группе пациенты не принимали НПВС и глюкокортикостероидные препараты как минимум за 1 мес до начала и в течение всего исследования. В контрольной группе пациенты получали курсами НПВС (в основном препараты амелотекс, вольтарен, найз), а также периодически по показаниям — инъекции глюкокортикостероидных препаратов (кеналог-40, дипроспан) на протяжении всего периода исследования.
Пациенты основной группы получали внутрисуставные инъекции ОТП. Приготовление и введение ОТП в коленный сустав пациента осуществляли в процедурном кабинете. Проводили забор 13–14 мл цельной крови из локтевой вены пациента с помощью 20 мл шприца. Затем цельную аутокровь сливали в герметично закрывающийся стерильный пластиковый контейнер YCELLBIO, добавляли 1,5 мл 5% раствор цитрата натрия и помещали в центрифугу с соответствующим противовесом. Первое центрифугирование проводили в течение 4 мин со скоростью 3600 об/мин, второе — со скоростью 3400 об/мин еще 4 мин. Плазму извлекали из контейнера с помощью шприца. Активацию ОТП препаратами кальция мы посчитали излишней, рассчитывая на естественный процесс эндогенной активации, который приводит к более пролонгированному эффекту регенерации [14]. Полученную взвесь вводили в полость коленного сустава при помощи 5 мл шприца с иглой 22G. Инъекции проводили 3-кратно с интервалом 1–2 нед.
Мы предполагали, что применение внутрисуставных инъекций ОТП повысит эффективность терапии остеоартроза коленных суставов за счет снижения выраженности болевого синдрома, повышения функциональных показателей, улучшения качества жизни пациентов. В связи с этим в работе использовали
4-балльную шкалу вербальной оценки эффективности лечения, визуально-аналоговую шкалу боли (ВАШ) и индекс тяжести гонартроза (шкала Лекена). Также регистрировали нежелательные явления, возникавшие в процессе лечения.
В обеих группах эффект лечения оценивали проспективно непосредственно перед началом лечения, через 1, 3 сут, 1, 3, 6 и 9 нед, 3, 4, 5 и 6 мес после лечения.
Все пациенты подписывали информированное согласие, в котором подробно объяснялась сущность процедуры, возможные риски и последствия лечения при использовании ОТП. Больные давали согласие на неприменение других видов лечения без согласования с врачом на протяжении 6 мес.
Для статистической обработки результатов исследования применяли электронные таблицы Excel 7.00, пакет статистических программ Statistica 6.0. Вычисляли средние, ошибку среднего, различия по t-критерию Стьюдента. Статистически значимыми считали различия при p<0,05.
Результаты
Полный курс лечения и наблюдения в основной группе прошли 50 (83%) человек, в контрольной — 54 (90%), 10 и 6 пациентов соответственно выбыли на различных сроках исследования по причинам, не связанным непосредственно с протоколом лечения.
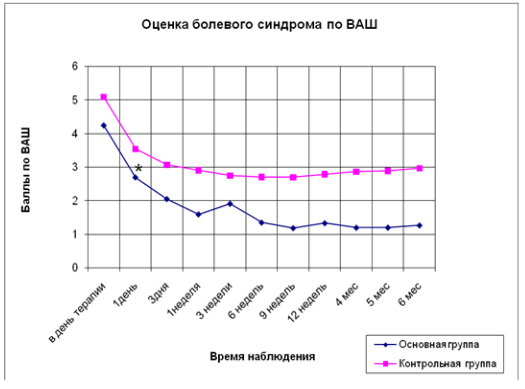
Средний показатель индекса боли ВАШ до начала лечения в основной группе составил 4,25±0,56 балла, в контрольной — 5,08±0,64 балла (см. рисунок, 1). Через 1 нед после начала лечения в основной группе индекс боли снизился до 1,6±0,5 балла, в контрольной — до 2,91±0,65 балла. К 3-му месяцу от начала лечения в основной группе наблюдалось снижение среднего показателя до 1,33±0,45 балла, в контрольной — до 2,8±0,67 балла. Через 6 мес в основной группе показатель составил 1,26±0,5 балла, т. е. снизился на 70%, в контрольной — 2,97±0,69 балла (снижение на 42%).
Рис.1. График изменения интенсивности болевого синдрома у пациентов основной и контрольной групп по шкале ВАШ в течение 6-ти месяцев наблюдения. *p<0,05.
Полное исчезновение боли через 6 мес после начала лечения в основной группе отметили 52% пациентов, в контрольной — 19%, на отсутствие динамики болевых ощущений по прошествии 6 мес указали 12 и 15% пациентов соответственно.
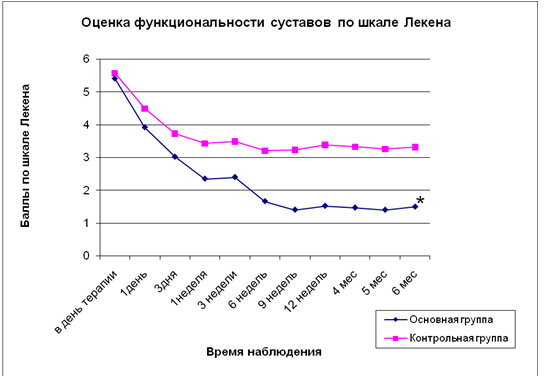
Средний показатель индекса Лекена на начала лечения у пациентов основной группы составил 5,43±0,85 балла, в контрольной — 5,57±0,91 балла (см. рисунок, 2). Через 1 нед после начала лечения в основной группе данный показатель снизился до 2,3 балла, в то время как в контрольной — до 3,42 балла. К 3-му месяцу средний показатель снизился до минимума, составив 1,52±0,47 и 3,38±0,8 балла в основной и контрольной группе соответственно. Через 6 мес пациенты обеих групп отмечали снижение дискомфорта при разных видах физической активности. В целом в основной группе исследуемый показатель снизился на 3,93 (с 5,43±0,85 до 1,5±0,5) балла, в контрольной — на 2,26 (с 5,57±0,91 до 3,31±0,8) балла. Через 6 мес после начала лечения в основной группе средний индекс Лекена достоверно снизился по сравнению с контрольной группой (p<0,05).
Рис.2. График изменения функциональных показателей тяжести течения гонартроза у пациентов основной и контрольной групп по шкале Лекена в течение 6-ти месяцев наблюдения. *p<0,05
Общая оценка степени удовлетворенности пациента результатом лечения осуществлялась пациентом и врачом по 4-балльной вербальной шкале оценки эффективности лечения. Согласно данной шкале 1 балл — отсутствие эффекта (улучшения нет, состояние такое же, как и до терапии), 2 балла — слабый эффект (есть незначительное улучшение), 3 балла — удовлетворительный эффект (значительное улучшение состояния, но меньше ожидаемого), 4 балла — хороший эффект (состояние пациента улучшилось в пределах или более ожидаемого).
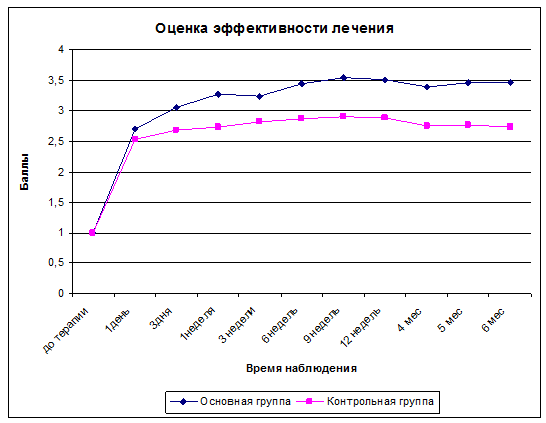
Средний показатель эффективности лечения до начала лечения как в основной, так и в контрольной группе составил 1 балл (см. рисунок, 3). На следующий день после начала лечения в основной группе этот показатель в среднем вырос до 2,72±0,26 балла, в контрольной — до 2,52±0,3 балла. В течение всего периода наблюдения значение индекса в группах находилось примерно на одном уровне (см. рисунок, 3). К концу срока наблюдения констатировали повышение оценки эффективности лечения в основной группе на 2,45 балла (от 1 до 3,45±0,21) от исходной, в контрольной — на 1,75 балла (от 1 до 2,75±0,29).
Рис.3. График изменения показателей эффективности лечения у пациентов основной и контрольной групп по вербальной шкале эффективности лечения в течение 6-ти месяцев наблюдения.
Нежелательные явления. Более трети (38%) пациентов к вечеру первых суток после введения ОТП отметили усиление боли (от 1 до 10 см по ВАШ). Однако уже на следующий день после введения 14 пациентов отмечали значимое уменьшение болевого синдрома.
В контрольной группе регистрировали нежелательные явления со стороны желудочно-кишечного тракта (16 (27%) пациентов), причем в 4 (7%) наблюдениях потребовалась замена или полная отмена препарата.
Обсуждения
Интраартикулярное введение ОТП с целью улучшения регенерации поврежденного гиалинового хряща при лечении пациентов с дегенеративными заболеваниями коленного сустава является современной, эффективной и перспективной методикой, активно используемой как в зарубежной, так и в отечественной медицине. Многие исследователи отмечают эффективность применения ОТП для купирования болевого синдрома уже на ранних этапах консервативного лечения патологии коленных суставах.
Д.А. Маланин и соавт. [9], проанализировав результаты лечения 81 пациента с гонартрозом, показали, что вводимая в сустав ОТП оказывала обезболивающее действие, что подтверждала оценка по ВАШ, причем у пациентов с III стадией гонартроза уменьшение выраженности болевого синдрома происходило путем кумуляции от первой инъекции к последней с максимальной положительной динамикой уже после первого введения. Субъективное ощущение обезболивания в группе ОТП к моменту завершения исследования изменилось на 4 балла против 2 баллов у пациентов, принимавших препараты из группы НПВС [9].
Kon и соавт. [11] в проспективном рандомизированном исследовании оценили результаты лечения 150 пациентов с гонартрозом путем трехкратного внутрисуставного введения ОТП в течение 3 нед. Высокая эффективность плазмы в отношении уменьшения выраженности боли и улучшения функции сустава в сроки до 6 мес была отмечена у пациентов с начальными стадиями гонартроза.
В работе [15] показатели выраженности боли и шкалы WOMAC у 52 пациентов с поражением коленных и тазобедренных суставов на первом и третьем месяце лечения снижались в обеих группах, хотя в группе с применением ОТП снижение показателей было более выраженным. И через 6 мес в основной группе пациентов показатели продолжали так же интенсивно снижаться, тогда как в контрольной группе практически не изменялись. Такая динамика показателей свидетельствует о том, что ОТП обладает пролонгированным эффектом и способна усиливать эффект от проведения стандартной терапии.
G. Görmeli и соавт. [10] отметили значительное облегчение болевого синдрома у пациентов, получавших 3-кратные инъекции ОТП, по сравнению с пациентами, которым однократно была введена аутоплазма или гиалуроновая кислота.
Необходимо отметить, что многие пациенты в нашем исследовании после 1-й инъекции ОТП отмечали усиление боли и дискомфорта к вечеру того же дня. Аналогичный эффект после введения ОТП наблюдали и другие исследователи [9, 11]. Однако на следующие сутки отмечено значимое улучшение состояния и снижение выраженности боли в среднем с 4,25 до 2,7 балла, т. е. на 36%. Через день после начала лечения в основной группе средний индекс боли достоверно снизился, по сравнению с таковым до начала лечения (p<0,05). Это свидетельствует о том, что инъекции ОТП обладают довольно быстрым обезболивающим эффектом, который проявляется через сутки после начала лечения.
В нашем исследовании наилучший показатель ВАШ был получен по прошествии 9 нед от начала лечения с применением ОТП, что совпадает с наблюдениями других исследователей [9, 16]. Средний показатель по группе составил 1,18±0,42 балла, что свидетельствует о значительном снижении болевого синдрома (более чем на 50%) по сравнению с состоянием пациентов до начала лечения. Наилучший результат в контрольной группе был отмечен через 6 нед после начала лечения и соответствовал 2,71±0,7 балла, при том, что до начала лечения средний балл был равен 5,08±1,1.
В рандомизированном контролируемом исследовании с участием 78 пациентов с гонартрозом не установлено достоверных различий в функциональных результатах после одной или двух внутрисуставных инъекций ОТП. Однако в обеих клинических группах результаты лечения были лучше, чем в группе с плацебо, но постепенно ухудшались в течение 6 мес [17].
По наблюдениям Д.А. Маланина и соавт. [9] динамика показателей по шкале Лекена за весь период наблюдения в значительной степени приближалась к таковой по ВАШ, поскольку основным критерием оценки в обеих шкалах является болевой синдром. Тем не менее уменьшение индекса тяжести гонартроза с 14 до 8 баллов свидетельствовало и о некотором улучшении функциональных возможностей коленного сустава. Тенденция к снижению индекса Лекена сохранялась от первой до третьей инъекции включительно, т.е. на протяжении 9 нед, что подчеркивало зависимость достигаемого эффекта от кратности введения ОТП.
Л.Ю. Широкова и соавт. [18] вводили ОТП в коленные суставы 83 женщинам в возрасте от 42 до 70 лет 2 раза в неделю в течение 3 нед и наблюдали за результатами в течение 3 мес. Авторы пришли к заключению о том, что выраженная положительная динамика характеризует функциональное состояние коленных суставов у лиц с начальными проявлениями остеоартроза только в течение 1 мес наблюдения. У пациенток с тяжелым гонартрозом, осложненным синовитом, лечение ОТП оказалось неэффективным.
По нашим данным, при оценке изменения функционального состояния коленных суставов в основной группе наилучший результат отмечен через 9 нед после первой инъекции, в контрольной группе он был достигнут несколько раньше — через 6 нед после начала лечения, однако снижение индекса Лекена было менее выраженным. Что касается полного восстановления функциональной активности сустава по результатам 6-месячного наблюдения, то его отметили 23 (46%) пациентов основной группы и лишь 11 (20%) — контрольной.
Оценке удовлетворенности пациента уделяется мало внимания, однако в работе [9] показана высокая степень удовлетворенности лечением с использованием внутрисуставного введения ОТП даже у пациентов с терминальными стадиями гонартроза. Количество респондентов, указавших на хороший и удовлетворительный результаты лечения ОТП, оказалось почти в 7 раз больше, чем в группе сравнения.
В нашем исследовании наибольшую удовлетворенность результатами лечения ОТП пациенты отметили через 9 нед после начала лечения. Средний показатель удовлетворенности вырос от 1 балла перед началом лечения до 3,55±0,17 балла к концу наблюдения. В контрольной группе наибольший средний показатель удовлетворенности результатами лечения также был отмечен через 9 нед после начала лечения и составил 2,9±0,27 балла. При оценке удовлетворенности пациентов лечением в основной группе наблюдалось значительное, почти в 2 раза, преобладание числа довольных пациентов по сравнению с контрольной группой (табл. 2). При этом средние показатели интенсивности болевого синдрома и функциональной активности в контрольной и основной группе на одних и тех же временных интервалах отличались незначительно. Вероятно, в данном случае большую роль сыграл психологический фактор нового, еще неиспробованного, но уже знаменитого способа лечения. Большинство пациентов основной группы изначально были настроены положительно, интересовались механизмом действия ОТП, с готовностью отвечали на вопросы при мониторинге состояния. В контрольной группе большинство пациентов относилось к процессу лечения скептически, так как многие уже не раз получали курсовое лечение НПВС без явного эффекта.
Табл. 2. Распределение пациентов в зависимости от оценки эффективности лечения по вербальной шкале эффективности через 6 мес после начала лечения
| Оценка | Основная группа | Контрольная группа |
| 1 балл | 4 (8%) | 6 (11%) |
| 2 балла | 3 (6%) | 18 (33%) |
| 3 балла | 10 (20%) | 11 (8%) |
| 4 балла | 33 (66%) | 19 (36%) |
Недостатком данного исследования является отсутствие слепого отбора, плацебо-контролируемой группы пациентов, отсутствие учета влияния разной степени остеоартроза у пациентов обеих групп, а также короткий период наблюдения.
Заключение
Применение ОТП для лечения остеоартроза коленных суставов II–III, III, III–IV стадии позволило снизить интенсивность болевого синдрома более чем вдвое за 6 мес, улучшить функцию сустава и существенно повысить эффективность лечения. Настоящее одноцентровое проспективное рандомизированное контролируемое исследование имеет уровень доказательности 2б. Результаты данного исследования позволяют рекомендовать использование ОТП в лечении остеоартроза коленных суставов как альтернативу НПВС, особенно при наличии противопоказаний к последним. Применение ОТП в лечении заболеваний коленных суставов дегенеративного характера является перспективным направлением в регенеративной медицине и требует дальнейшего всестороннего изучения.
Литература [References]
- Бадокин В.В. Современные аспекты патогенетической терапии остеоартроза. Медицинский совет. 2013; 12: 77–83 [Badokin V.V. Modern aspects of the pathogenetic therapy of osteoarthritis. Meditsinskiy sovet. 2013; 12: 77-83 (in Russian)].
- Алексеева Л.И., Верткин А.Л., Иванов В.С. Остеоартроз в практике врача-терапевта. Русский медицинский журнал. 2008; 16 (7): 476–80 [Vertkin A.L., Alekseeva L.I., Naumov A.V., Ivanov V.S., Shamuilova M.M., Mendel’ O.I. Osteoarthrosis in practice of the physician. Russkiy meditsinskiy zhurnal. 2008; 16 (7): 476-80 (in Russian)].
- Алексеева Л.И. Современные представления о диагностике и лечении остеоартроза. Русский медицинский журнал. Ревматология. 2000; 9: 81–8 [Alekseeva L.I. Modern conceptions on osteoarthrosis diagnosis and treatment. Russkiy meditsinskiy zhurnal. Revmatologiya. 2009; 9: (7): 81-8 (in Russian)].
- Holt H.L., Katz J.N., Reichmann W.M., Gerlovin H., Wright E.A., Hunter D.J. et al. Forecasting the burden of advanced knee osteoarthritis over a 10-year period in a cohort of 60-64 year-old US adults. Osteoarthritis Cartilage. 2011; 19 (1): 44-50.
- Bruyere O., Cooper C., Pelletier J.P. An algorithm recommendation for the management of knee osteoarthritis in Europe and internationally: A report from a task force of the European Society for Clinical and Economic Aspects of Osteoporosis and Osteoarthritis (ESCEO). Semin. Arthritis Rheum. 2014; 44 (3): 253–63.
- Миронов С.П. Очкуренко А.А., Кесян Г.А. Савельев С.Н., Аркадьев А.А., Збараг Н.Н. Эффективность применения аутологичных факторов роста при повреждениях и заболеваниях костно-мышечной системы. Вестник травматологии и ортопедии им. Н.Н. Приорова. 2014; 1: 86–93 [Mironov S.P., Ochkurenko A.A., Kesyan G.A., Savel’ev S.N., Arkad’ev A.A., Zbarag N.N. Efficacy of autologous growth factors application in musculo-skeletal system injuries and diseases. Vestnik travmatologii i ortopedii im. N.N. Priorov. 2014; 1: 86-93 (in Russian)].
- Haleem A.M., Singergy A.A., Sabry D., Atta H.M., Rashed L.A., Chu C.R. et al. The Clinical use of human culture–expanded autologous bone marrow mesenchymal stem cells transplanted on platelet-rich fibrin glue in the treatment of articular cartilage defects: A pilot study and preliminary results. Cartilage. 2010; 1 (4): 253–61.
- Castricini R., Longo U.G., De Benedetto M..Platelet-rich plasma augmentation for arthroscopic rotator cuff repair. A randomized controlled trial. Am. J. Sports. Med. 2011; 39: 258–65.
- Маланин Д.А., Новочадов В.В., Демкин С.А., Демещенко М.В., Данилов Д.И. Обогащенная тромбоцитами аутологичная плазма в лечении пациентов с гонартрозом 3 стадии. Травматология и ортопедия России. 2014; 3 (73): 57–65 [Malanin D.A., Novochadov V.V., Dyomkin S.A., Demeshchenko M.V., Danilov D.I. Autologous platelet-rich plasma in the treatment of patients with knee arthritis iii stage. Travmatologiya i ortopediya Rossii. 2014; 3 (73): 57-65 (in Russian)].
- Görmeli G., Görmeli C.A., Ataoglu B., Çolak C., Aslantürk O., Ertem K. Multiple PRP injections are more effective than single injections and hyaluronic acid in knees with earlyosteoarthritis: a randomized, double-blind, placebo-controlled trial. Knee Surg. Sports. Traumatol. Arthrosc. 2015; 2: 1–8.
- Filardo G., Di Matteo B., Di Martino A., Merli M.L., Cenacchi A., Fornasari P., Marcacci M., Kon E. Platelet-rich plasma intra-articular knee injections show no superiority versus viscosupplementation: A randomized controlled trial. Am. J. Sports Med. 2015; 43 (7): 1575–82.
- Khoshbin A., Leroux T., Wasserstein D., Marks P., Theodoropoulos J., Ogilvie-Harris D., Gandhi R., Takhar K., Lum G., Chahal J. The efficacy of platelet-rich plasma in the treatment of symptomatic knee osteoarthritis: a systematic review with quantitative synthesis. Arthroscopy. 2013; 29 (12): 2037–48.
- Forogh B., Mianehsaz E., Shoaee S., Ahadi T., Raissi G.R., Sajadi S. Effect of single injection of Platelet-rich plasma in comparison with corticosteroid on knee osteoarthritis: a double-blind randomized clinical trial. J. Sports Med. Phys. Fitness. 2015; 14 [Epub ahead of print].
- Detterline A.J., Goldberg S., Bach B.R. Jr, Cole B.J. Treatment options for articular cartilage defects of the knee. Orthop. Nurs. 2005; 24: 361.
- Емелин А.Л., Ахтямов И.Ф. Клиническая эффективность тромбоцитарной аутоплазмы при лечении остеоартрозов. Вестник современной клинической медицины. 2013; 6 (1): 26–9 [Emelin A.L., Akhtyamov I.F. Clinical efficacy platelet-rich autoplasma in treatment of osteoporosis. Vestnik sovremennoy klinicheskoy meditsiny. 2013; 6 (1): 26-9 (in Russian)].
- Campbell K.A., Saltzman B.M., Mascarenhas R., Khair M.M., Verma N.N., Bach B.R.Jr, Cole B.J. Does intra-articular Platelet-Rich Plasma injection provide clinically superior outcomes compared with other therapies in the treatment of knee osteoarthritis? A systematic review of overlapping meta-analyses. Arthroscopy. 2015; 31 (11): 2213–21.
- Patel S., Dhillon M.S., Aggarwal S., Marwaha N., Jain A. Treatment with platelet-rich plasma is more effective than placebo for knee osteoarthritis: а prospective, double-blind, randomized trial. Am. J. Sports Med. 2013; 41: 356–64.
- Широкова Л.Ю., Носков С.М., Бахтиарова Т.И., Снегирева А.В., Носкова Т.С. Локальная терапия гонартроза аутологичной, обогащенной тромбоцитами плазмой. Современные технологии в медицине. 2012; 1: 97–100 [Shirokova L.Yu., Noskov S.M., Bakhtiarova T.I., Snegiryova A.V., Noskova T.S. Local (in therapy of gonarthrosis with platelet-rich autoplasma. Sovremennye tekhnologii v meditsine. 2012; 1: 97-100 (in Russian)].
Сведения об авторах
Горбатенко А.И. — канд. мед. наук, доцент кафедры травматологии и ортопедии;
Костяная Н.О. — биолог лаборатории молекулярной генетики ГУЗ РОПАБ.
Контакты
Горбатенко Андрей Иванович. Россия, 344022, Ростов-на-Дону, пер. Нахичеванский, д. 29, Тел.: +7 (918) 556–24–41. E-mail: gorbatenkophmd@gmail.com.